Johtavuuselektrodit on tarkoitettu erityisesti puhtaan veden, ultrapuhtaan veden, vedenkäsittelyn jne. johtavuusarvon mittaamiseen. Ne sopivat erityisesti johtavuusmittauksiin lämpövoimalaitoksissa ja vedenkäsittelyteollisuudessa. Niille on ominaista kaksoislieriörakenne ja titaaniseosmateriaali, joka voidaan hapettaa luonnollisesti kemiallisen passivoinnin aikaansaamiseksi. Sen tunkeutumisenestoinen johtava pinta kestää kaikenlaisia nesteitä paitsi fluoridihappoa. Lämpötilakompensointikomponentit ovat: NTC2.252K, 2K, 10K, 20K, 30K, ptl00, ptl000 jne., jotka käyttäjä määrittää. K=10.0- tai K=30-elektrodi on valmistettu suuresta platinarakenteesta, joka kestää vahvoja happoja ja emäksiä ja jolla on vahva saastumisenestokyky. Sitä käytetään pääasiassa johtavuusarvon online-mittaukseen erikoisteollisuudessa, kuten jätevedenpuhdistusteollisuudessa ja meriveden puhdistuksessa.
| Elektrodin vakio | 0,1 | 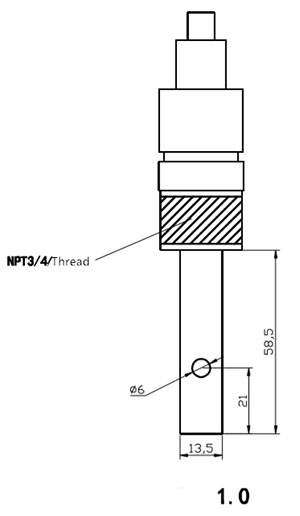 |
| Puristuslujuus | 0,6 MPa | |
| Mittausalue | 0–200 μS/cm | |
| Yhteys | 1/2 tai 3/4 kierteen asennus | |
| Materiaali | 316L ruostumaton teräs | |
| Hakemus | Vedenkäsittelyteollisuus |
Johtavuuson veden kyvyn mitta sähkövirran läpi kulkemisessa. Tämä kyky liittyy suoraan veden ionipitoisuuteen.
1. Nämä johtavat ionit ovat peräisin liuenneista suoloista ja epäorgaanisista aineista, kuten emäksistä, klorideista, sulfideista ja karbonaattiyhdisteistä
2. Ioneiksi liukenevia yhdisteitä kutsutaan myös elektrolyyteiksi 40. Mitä enemmän ioneja on läsnä, sitä suurempi on veden johtavuus. Samoin mitä vähemmän ioneja vedessä on, sitä huonommin se johtaa sähköä. Tislattu tai deionisoitu vesi voi toimia eristeenä erittäin alhaisen (ellei jopa merkityksettömän) johtavuusarvonsa vuoksi. Merivedellä puolestaan on erittäin korkea johtavuus.
Ionit johtavat sähköä positiivisten ja negatiivisten varaustensa ansiosta
Kun elektrolyytit liukenevat veteen, ne jakautuvat positiivisesti varautuneiksi (kationeiksi) ja negatiivisesti varautuneiksi (anioneiksi) hiukkasiksi. Kun liuenneet aineet jakautuvat vedessä, sekä positiivisen että negatiivisen varauksen pitoisuudet pysyvät samoina. Tämä tarkoittaa, että vaikka veden johtavuus kasvaa lisättyjen ionien myötä, se pysyy sähköisesti neutraalina.






















